一、何为抗原检测产品
据观研报告网发布的《中国抗原检测行业发展趋势分析与未来前景调研报告(2022-2029年)》显示,传染病的检测方法可分为三种:核酸检测、抗原检测和抗体检测。核酸检测、抗原检测直接检测病原体,抗体检测通过间接检测被病原体入侵后产生的抗体而获得间接证据。核酸检测常用荧光定量RT-PCR方法。PCR通过变温反应扩增目的脱氧核糖核酸片段,以荧光信号检测每次PCR循环后产物的总量,特定的探针可与脱氧核糖核酸片段结合产生荧光信号,以荧光信号的积累情况可以判断样本中是否存在目标病毒核酸片段。核酸检测直接检测核酸的特异基因,是传染病筛查确诊的金标准。一个完整的RT-PCR历时3-5小时,故核酸检测出结果需3小时以上时间。
| 传染病的检测方法 |
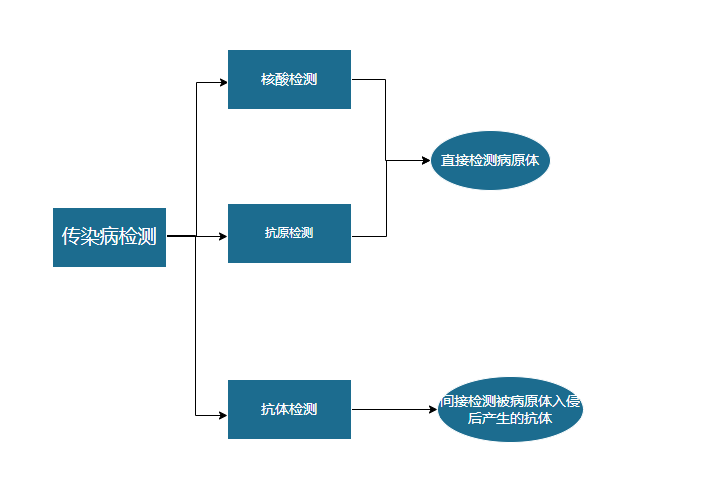
资料来源:观研天下数据中心整理
抗原检测是通过抗原和抗体结合反应在试纸条上检测,方便快捷,一般15-20分钟即可出结果。但抗原抗体反应因为会有一些干扰的存在而出现假阳性,方法学上的特异性达不到100%。所以,抗原检测结果不可替代核酸检测结果。
在新冠病毒感染人体后,能刺激浆细胞产生特异性抗体,借助抗原和抗体在体外特异结合后出现的各种现象,可以对样品中的抗原或抗体进行定性、定量、定位的检测。用已知的抗体和待检样品混合,经过一段时间,若有免疫复合物形成的现象发生,就说明待检样品中有相应的抗原存在(阳性)。若无预期的现象发生,则说明样品中无相应的抗原存在(阴性)。
| 双抗体夹心法检测抗原的胶体金试纸原理 |
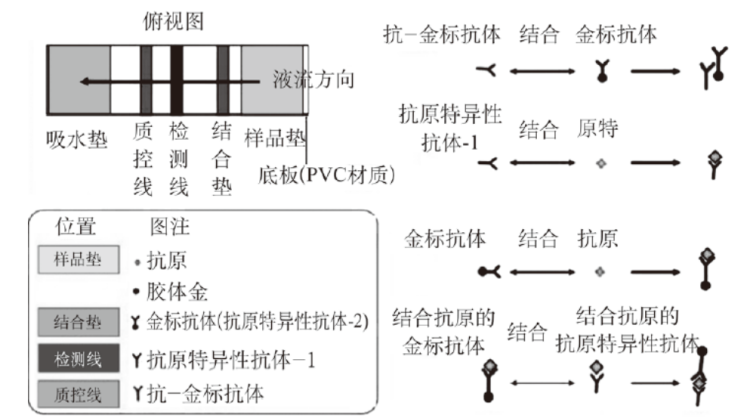
资料来源:新冠病毒抗原检测应用方案(试行),观研天下数据中心整理
| 抗原自测的步骤 |
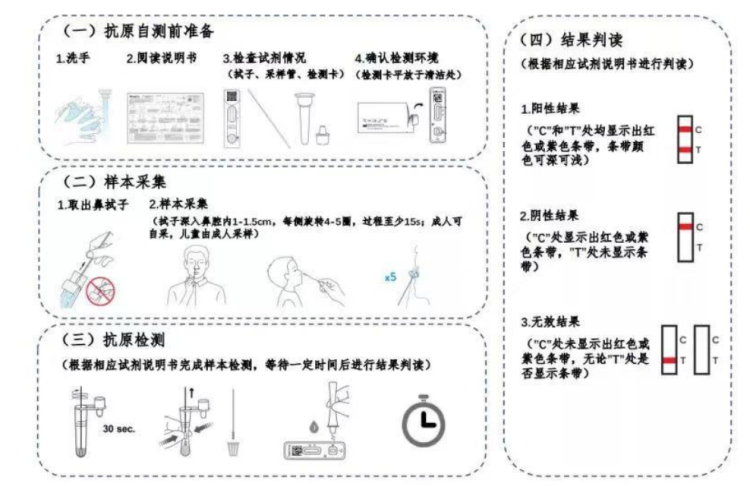
资料来源:新冠病毒抗原检测应用方案(试行),观研天下数据中心整理
二、新冠疫情持续蔓延,激发抗原检测产品需求
在当前形势下,新冠疫情依然在全球蔓延,变异株Omicron传染性极强,海外多国疫情反复,确诊人数持续增加。
根据Worldometer实时统计数据,截至北京时间2022年3月29日6时30分左右,全球累计确诊新冠肺炎病例482771128例,累计死亡病例6150581例。全球单日新增确诊病例917666例,新增死亡病例2802例。
其中,韩国、法国、澳大利亚、日本、意大利是新增确诊病例数最多的五个国家。俄罗斯、韩国、德国、美国、法国是新增死亡病例数最多的五个国家。
韩国新增超18万例确诊病例25天来首次降至20万例以下
韩国疾病管理厅28日通报,截至28日零时,韩国前一日新增新冠确诊病例约18.7万例,25天来单日新增首次降至20万例以下。与此同时,韩国累计新冠确诊病例突破1200万例。韩国新增死亡病例287例,较前一日增加5例。
法国新增超2.9万例确诊病例累计确诊逾2505万例
截至当地时间28日,法国累计新冠肺炎确诊病例达25059058例,过去24小时内新增29455例;累计死亡病例达141823例,过去24小时内新增151例。
美国新增超1.5万例确诊病例白宫新闻副发言人新冠检测结果呈阳性
根据Worldometer实时统计数据,截至北京时间2022年3月29日6时30分左右,美国累计确诊新冠肺炎病例81634470例,累计死亡病例1003760例;与前一日6时30分左右数据相比,美国新增确诊病例15582例,新增死亡病例330例。
俄罗斯新增超2万例确诊病例累计确诊逾1778万例
俄罗斯新冠病毒疫情防控指挥部28日表示,过去24小时,新增新冠病毒感染病例21101例,累计感染病例达17783843例。新增死亡病例335例,全国累计死亡病例为367686人。
| 全球疫情分布情况 |
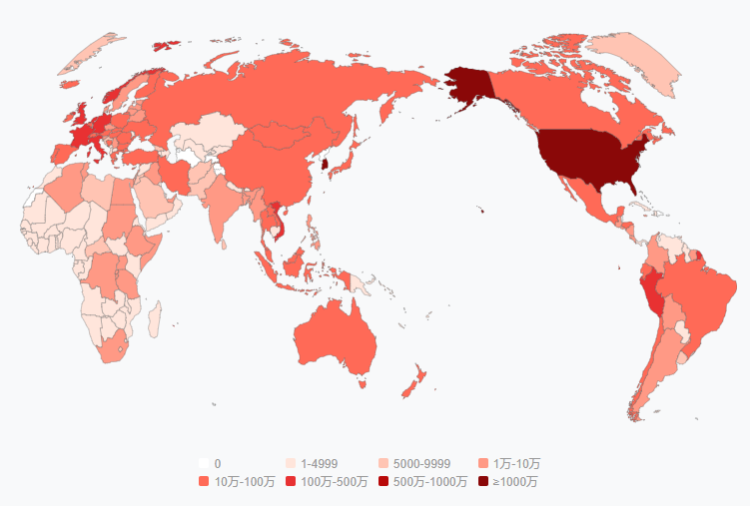
数据来源:百度疫情数据,数据截止2022年3月28日
从全球范围来看,随着变异株传染性增强,各国加快抗原自测试剂获批上市,其中,德国在2021年率先推行新冠抗原居家检测,并颁布相应自测准入资质Bfarm。随着新冠变异毒株传染力增强,疫情扩散,其他欧洲国家也相继推出本地的自测资质。
美国于2021年7月,陆续公布通过新冠抗原试剂盒FDA、EUA的厂家,截至22年3月共有28家公司,45款产品通过美国FDAEUA,目前,美国EUA批准的新冠抗原检测试剂产品共计45个,家用16个,专业29个。其中2022年3个,2021年31个,2020年11个。有抗原检测产品获批的企业28家,国产企业3家,分别是东方生物、艾康生物和九安医疗,有9家企业获批数2个及以上。
日本、韩国和新加坡政府也在加速批准抗原自测试剂上市,重视抗原自测的筛查作用。其中,日本抗原试剂开始批准的时间较早,第一个获批产品于20年5月上市,至今为止共有44项产品获批,平均每月获批2项。2022年2月共7项产品获得批准,推测和奥密克戎毒株散布有关。其中,2022年2月10日,中国亚辉龙生产的新冠抗原试剂盒产品取得日本PMDA认证批准上市。
韩国:于20年11月开始批准抗原检测产品,至今共有42项产品在国内上市。今年2月疫情加剧严重,政府单月批准了7项抗原产品供给抗疫。
新加坡:目前共批准21项产品。今年1、2月各批准了3项,目前3月尚未过半,已经批准4项。其中,中国企业热景生物本月11日晚间公告称,已获得新加坡卫生科学局(HSA)批准新冠抗原检测试剂一项,后续可在新加坡和认可新加坡(HSA)认证的国家及地区进行销售。
三、抗原检测产品有望成为“居家消费品”
在新冠疫情的驱动下,抗原检测产品需求增加,各国抗原检测产品审批速度加快。从短期来看,新冠抗原自测试剂可以助力疫情的早期筛查,是核酸检测试剂的有益补充。但从长期来看,新冠抗原自测试剂有望成为“居家消费品”。
以德国为例,德国是家用抗原自测的开辟者,截止2022年3月,经过BfArM检测的CE认证(或没有通过CE认证但通过BfArM特别批准)的抗原产品共672种,包括608种专业抗原产品和64种家用抗原产品。其中有456种中国抗原产品,包含了410种专业抗原和46种家用抗原。
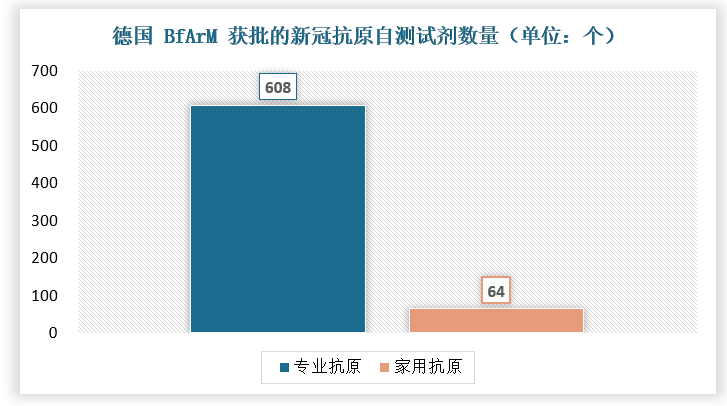
数据来源:BfArM,观研天下数据中心整理
从我国来看,为了应对疫情变化,我国不断加快推动家用抗原检测产品获批。2022年3月11日,《新冠病毒抗原检测应用方案(试行)》发布,为进一步优化新冠病毒检测策略,服务疫情防控需要,经研究,国务院应对新型冠状病毒肺炎疫情联防联控机制综合组决定在核酸检测基础上,增加抗原检测作为补充,并组织制定了的方案。方案指出社区居民有自我检测需求的,可通过零售药店、网络销售平台等渠道,自行购买抗原检测试剂进行自测。
2022年3月12日,国家药监局发布通告,批准南京诺唯赞、北京金沃夫、深圳华大因源、广州万孚生物、北京华科泰生物的新冠抗原产品自测应用申请变更。自此五款新冠抗原自测产品正式上市。
之后国家药监局又批准5家新冠抗原检测试剂盒产品的注册申请,这5家企业包括北京万泰生物药业股份有限公司、北京热景生物技术股份有限公司、天津博奥赛斯生物科技股份有限公司、重庆明道捷测生物科技有限公司、北京乐普诊断科技股份有限公司。
2022年3月15日晚,国家药监局批准武汉明德生物科技股份有限公司、浙江东方基因生物制品股份有限公司的新冠抗原自测产品的注册申请。
2022年3月16日晚上,国家药监局审批通过了艾康生物技术(杭州)有限公司的新冠抗原自测产品的注册申请。
2022年3月17日,经国家药监局审查,批准中元汇吉生物技术股份有限公司的新冠病毒抗原检测试剂产品的注册申请。
2022年3月18日,山东康华生物&青岛汉唐生物研制的新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)获得国家药监局批准正式上市,这是山东首个获批上市的新冠病毒抗原检测试剂盒。
目前,我国药监局共批准新冠病毒检测试剂80多个(包括34个核酸检测试剂、31个抗体检测试剂、17个抗原检测试剂)。
|
2022年中国部分新型冠状病毒抗原检测试剂盒产品 |
||
|
时间 |
产品名称 |
申请公司 |
|
2022/03/11 |
新型冠状病毒(2019-nCoV)抗原检测试剂盒(荧光免疫层析法) |
北京华科泰生物技术股份有限公司 |
|
2022/03/12 |
新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法) |
南京诺唯赞医疗科技有限公司 |
|
新型冠状病毒(2019-nCoV)抗原检测试剂盒(乳胶法) |
北京金沃夫生物工程科技有限公司 |
|
|
新型冠状病毒(2019-nCoV)抗原检测试剂盒(荧光免疫层析法) |
深圳华大因源医药科技有限公司 |
|
|
新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法) |
广州万孚生物技术股份有限公司 |
|
|
2022/03/13 |
新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法) |
北京万泰生物药业股份有限公司 |
|
新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法) |
北京热景生物技术股份有限公司 |
|
|
新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法) |
天津博奥赛斯生物科技股份有限公司 |
|
|
新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法) |
重庆明道捷测生物科技有限公司 |
|
|
2022/03/15 |
新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法) |
武汉明德生物科技股份有限公司 |
|
新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法) |
浙江东方基因生物制品股份有限公司 |
|
|
2022/03/16 |
新型冠状病毒(2019-nCoV)抗原检测试剂盒(乳胶法) |
艾康生物技术(杭州)有限公司 |
|
2022/03/17 |
新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法) |
中元汇吉生物技术股份有限公司 |
资料来源:观研天下数据中心整理
当前疫情防控已经进入常态化,各地需要频繁进行核酸检测,而家用抗原检测作为补充手段可以用于人群的筛查,提高疫情防控能力。未来随着家用抗原检测产品的推出,抗原检测将有望成为居家必备的检测产品,基于我国的人口数量,家用抗原检测将有较大增长空间,具备产品力和品牌优势的企业有望占据优势。

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。