疫苗是指为了预防、控制传染病的发生、流行,用于人体预防接种的疫苗类预防性生物制品。对个人而言,疫苗的接种能够保护自身免受疾病威胁;对社会而言,疫苗接种能够减少卫生总支出,具备很高的经济效益,疫苗接种费用远低于疾病发生后所产生的高额医疗费用,同时也减少了因疾病导致的经济损失和社会危害。
根据观研报告网发布的《中国疫苗行业发展深度分析与投资前景预测报告(2022-2029年)》显示,目前,已有超过20种高危疾病可以通过疫苗接种得到有效预防。根据病原体的种类,疫苗大致可分为细菌性疫苗和病毒性疫苗。常见的细菌性疫苗包括卡介苗、霍乱疫苗、百白破疫苗、流脑疫苗、B型流感嗜血杆菌疫苗、肺炎疫苗等;常见的病毒性疫苗包括乙肝疫苗、乙脑疫苗、甲肝疫苗、麻腮风疫苗、水痘疫苗、轮状病毒疫苗、流感疫苗、HPV疫苗等。

资料来源:观研天下整理
1、市场现状
2002年以前,中国普通人群中乙肝病毒感染的比例高达57%,相当于每10个人中就有1人是乙肝病毒携带者,随着乙肝疫苗的普及,约5000万人免于成为慢性乙肝病毒感染者,1250万人免于因乙肝病毒感染相关疾病而发生过早死亡。
1950-1977年间,我国每年约报告1.1万-4.4万例脊灰病例,自1978年通过普及脊灰疫苗的接种,儿童脊灰发病和死亡率大幅度下降。
1950-1965年间,我国麻疹平均每年发病数接近400万例、死亡数超过6万例,从1965年起,我国开始使用麻疹疫苗,1978年纳入儿童计划免疫,2020年,全国麻疹发病降到历史最低水平,发病率仅为0.061/10万。
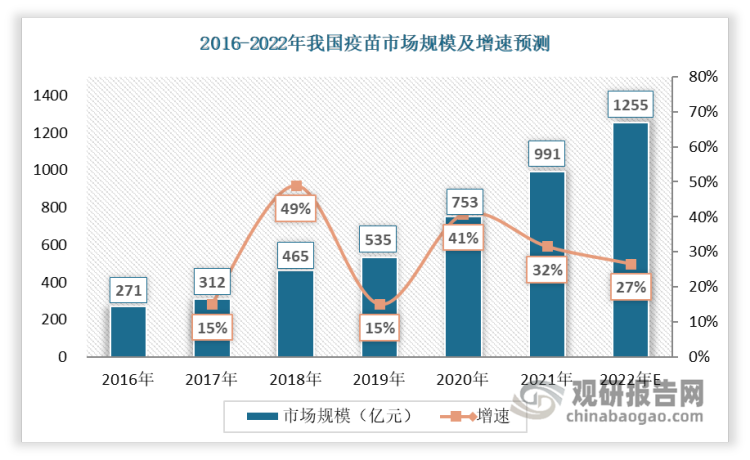
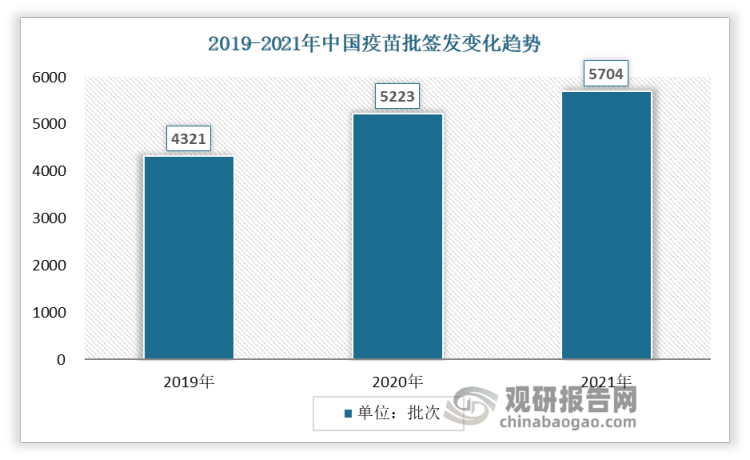
几十年以前,许多人会因为长痘、腹泻、伤寒等“小病”失去生命,然而现在,人类已利用疫苗控制了天花、百日咳、白喉、破伤风、脊髓灰质炎等多种疾病,疫苗为人类生命健康筑起了一道预防疾病的绿色屏障,让千千万万人免受传染病的侵扰。2021年,中国疫苗市场规模达991亿元,行业总计实现批签发5704批次,较去年同期增长9.2%。
资料来源:观研天下整理
资料来源:观研天下整理
发病率决定了赛道的规模,从细分产品来看,目前,水痘、狂犬病、流感、百白破、HPV、新冠等疾病的疫苗市场规模较大。计划免疫疫苗由政府招标采购,价格低廉,利润不高,市场基本稳定,目前主要由国内疫苗生产商供应。计划外市场呈寡头垄断格局,美国辉瑞、默沙东、英国葛兰素史克和法国赛诺菲四大制药巨头研发实力强,原创性疫苗多,占据了近90%的市场份额,国内竞争格局为中生集团六大研究所(北京、兰州、长春、武汉、上海、成都)及医科院昆明所长期占据着行业主导地位,其他企业积极参与。从疫苗品种看,2020 年全球销量前十的产品全部由四家疫苗巨头公司生产,但随着我国疫苗企业在技术研发、产品布局、产能建设等多方面快速发展,国产疫苗正走向国际市场,市场空间将进一步得到拓展。
2、发展历程
疫苗的诞生最早可以追溯到18世纪。在中国唐朝,一种名叫天花的病毒非常猖狂,名医孙思邈用取自天花患者口疮中的脓液敷在皮肤上来预防天花,到明代以后,出现了以接种天花患者的脓液,这种接种人痘的独创性方法来预防天花,后来,这种方法在18世纪初期传播到了欧洲,一名英国医生爱德华詹纳发明了牛痘接种术,成功制作出了天花疫苗。自此,狂犬病疫苗、霍乱疫苗等开始不断问世。
我国疫苗行业发展历程从 50 年代普种牛痘苗开始正式建立计划免疫体系,到现如今计划免疫体系在各城乡已经较为成熟,这其中经历了70多年的努力,按照计划免疫规划进度来看,可分为五个阶段,21世纪初期,我国已经成功实现了用14种疫苗预防15种疾病的目标,全国平均接种率达到85%。
我国疫苗行业发展历程
|
时间 |
|
|
1950-1977年(计划免疫前期) |
该阶段做较多的准备工作,如建设预防网络、建预防接种卡片等,还在农村建立接种登记、加强宣传教育,计划免疫的雏形初步落实。 |
|
1978-2002年(计划免疫初期) |
这一时期我国陆续开始实行免疫规划,最早的免疫规划程序包括“四苗六病”:包含的四种疫苗是:卡介苗,脊灰疫苗OPV,百白破疫苗及卡介苗;预防的六种疾病为:结核病、脊灰、百日咳、白喉、破伤风和麻疹。2002年一类苗范围扩大到6种,增加了乙肝疫苗与白破疫苗。 |
|
2003-2007年(计划免疫探索期1 ) |
该阶段疫苗品种大幅增加。2007年,我国已有14种疫苗预防15种疾病了。增加了四类儿童免疫规划疫苗:甲肝疫苗,流脑疫苗,乙脑疫苗,麻腮风疫苗,以及三类重点人群接种的疫苗:出血热疫苗,炭疽疫苗与钩体疫苗。 |
|
2008- 2019年(计划免疫探索期2) |
2016年5月1日起,新的脊灰疫苗免疫策略开始实施,停用三价脊灰减毒活疫苗(tOPV) ,用二价脊灰减毒活疫苗(bOPV)替代tOPV,并将脊灰灭活疫苗(IPV)纳入国家免疫规划。2019年12月起,脊灰疫苗的接种由1剂IPV+3剂bOPV调整为2剂IP+2剂bOPV。 |
|
2020年-至今(计划免疫探索期3 ) |
自从新冠疫情发展至今,中国新冠疫苗系列陆续通过审批,新冠疫苗的研发也在一定程度上提供中国疫苗研发技术的升级和产业进步。 |
资料来源:观研天下数据中心整理
目前,关于疫苗还有很多误解。
误解一:疫苗是否安全?
先来看看疫苗是什么?
疫苗是将病原微生物(如细菌、立克次氏体、病毒等)及其代谢产物,经过人工减毒、灭活或利用转基因等方法制成的用于预防传染病的自动免疫制剂。
这个过程中保留了病原菌刺激动物体免疫系统的特性。当动物体接触到这种不具伤害力的病原菌后,免疫系统便会产生一定的保护物质,如免疫激素、活性生理物质、特殊抗体等;当动物再次接触到这种病原菌时,动物体的免疫系统便会依循其原有的记忆,制造更多的保护物质来阻止病原菌的伤害。
在疾病没有发生之前,可以用来预防疾病、降低发病、死亡风险的。目前我国疫苗可分为“一类苗”和“二类苗”,一类苗是免费接种,政府买单。二类苗是民众自愿接种,自己买单。这两种疫苗在上市前要经过研发阶段、注册阶段、生产阶段、流通阶段、使用阶段五个时期,通过严格的动物实验和临床研究,每个环节都有严格复杂的药政审批程序的监督。特别是国家实行生物制品批签发制度以来,以往在各个环节中相对时间最短的生产阶段,也延长了时间,因为产品不仅需要企业检定合格后才能出厂,还需要国家检定所的合格报告在生产过程中经过了严格的质控管理,成品经过了严格的质量检验,因此都是安全的。
我国疫苗从研发到上市的五个环节
|
阶段 |
介绍 |
|
研发阶段 |
指的是上市注册申报之前的所有阶段,具体又分为几个不同的环节:1.概念验证阶段2.立项研究3.安评4.IND 5.临床I期6.临床II期7.临床III期。 |
|
注册阶段 |
完成临床实验揭盲获得完整的报告之后,如果有效性和安全性达到预期,且生产质量可控,就可以申报疫苗产品注册。 药品注册,是指国家食品药品监督管理局根据药品注册申请人的申请,依照法定程序,对拟上市销售药品的安全性、有效性、质量可控性等进行审查,并决定是否同意其申请的审批过程。而疫苗属于预防性生物制品,申请更加严格,准备的资料更多,基本上需要从上面说的立项开始的所有资料都要好好准备。并且疫苗不可以外包,必须自己申报自己建厂产,所以还有厂房的各项管理设施是否可以做到质量可控,试生产的产品是否达到预期等,一般光这个过程就要大约两年。拿到注册批件之后,企业才能开足马力开始生产。 |
|
生产阶段 |
这一阶段相对比较容易理解,就是按照已批准的工艺流程进行生产、检定、灌装等操作。待生产出产品后,还需要送至中国食品药品检定研究院以及药品检定所进行抽样鉴定。检定合格后拿到合格证,产品方可上市销售。 |
|
流通阶段 |
这一阶段主要就是销售以及产品发运的过程。大部分疫苗都需要2-8°C冷藏保存。因此在运输过程中药品的冷链运输也是非常重要的。国家在2013年底出台新版GSP、也就是《药品经营质量管理规范》,来规定疫苗这类冷链产品在发运过程中的温度保证。 |
|
使用阶段 |
使用阶段需要注意的是,现在疫苗全部采用批签发和一票制。批签发是指:是对获得上市许可的疫苗类制品、血液制品等,在每批产品上市销售前或者进口时,指定药品检验机构进行资料审核、现场核实、样品检验的监督管理行为。一票制指: 厂家生产的二类疫苗需要首先在省平台招标挂网,挂网后去疾控可以在省疾控的二类疫苗采购平台下单,下单后由医药商业公司负责送货至去疾控,最后再由区疾控至疫苗接种点。疫苗流通环节已经没有了经销商,企业自身其实也不用去销售。以上是针对二类疫苗,相当于居民自费的商业疫苗。对于一类计划免疫疫苗,国内都是有中生集团生产供货,属于垄断但不怎么盈利,带有社会主义优越性的产品,免费接种。 |
资料来源:观研天下数据中心整理
误解二:国外疫苗有效率是95%,国内的只有不到80%,是不是外国疫苗更好?
有效率不是衡量疫苗好不好唯一的标准。疫苗用在健康的人身上,和药物不一样,药物是为了就急,疫苗最重要的是有效性和安全性,对不良反应的容忍性更小,另外还要考虑研发难度、产能等,为保证疫苗的安全性和有效性,疫苗临床试验入组人数更多,安全性评价周期更长,疫苗的研发周期更长、研发费用也相应更高。例如:登革热疫苗研制出来使用不到两年就出现了许多新问题,这相当于是研发失败,第一个出血热疫苗用了近十年的时间才能算得上成功。从技术路线的角度来看:国内传统灭活疫苗技术路径成熟,研发速度快,不良反应更少且能保障可靠的供应。国外比较推崇基因编辑疫苗,这是比较新的技术,生产灵活,但是存在局部不良反应和全身不良反应发生率较高等问题。通常情况下,一款疫苗从研发到上市往往需要10-15年甚至20-30年时间,因此很难单纯比较哪个疫苗更好,判断疫苗的好坏要具体产品具体分析,综合效率、安全性(有无不良反应、有的话多大)、经济性、储藏和运输、生产周期、供给速度等多种指标进行判断。
不同技术路线疫苗影响生产成本和量产的主要因素对比
|
技术路线 |
体外培养病毒 |
诱导细胞免疫 |
量产速度 |
人体安全性 |
|
灭活疫苗 |
是 |
否 |
弱 |
强 |
|
减毒疫苗 |
是 |
是 |
弱 |
弱 |
|
重组亚单位疫苗 |
否 |
否 |
强 |
强 |
|
腺病毒载体疫苗 |
是 |
是 |
弱 |
强 |
|
核酸疫苗 |
否 |
是 |
极强 |
未知 |
资料来源:观研天下数据中心整理
3、行业机遇
在中国,疫苗行业的机遇在哪里?
政策端来看,“十二五”以来,将生物产业列为七大战略性新兴产业之一,其中强调了疫苗是生物产业的重点发展方向,“十四五”时期,规划更是提出紧跟疫苗技术发展趋势,基于应对新发、突发传染病需求,支持建设新型病毒载体疫苗、脱氧核糖核酸( DNA )疫苗、信使核糖核酸( mRNA )疫苗、疫苗新佐剂和新型递送系统等技术平台,推动相关产品的开发和产业化。近年来,我国陆续颁布出台了《疫苗管理法》等一系列相关法律法规,实行高于药品之上的最严管理,在强监管背景下,我国疫苗行业长期发展前景可期。
我国疫苗行业相关政策汇总
|
文件名称 |
发文时间 |
有关部门 |
主要内容 |
|
《关于做好2021-2022年流行季流感防控工作的通知》 |
2021-10 |
/ |
为保证接种人群得到最大程度保护,即使流感疫苗组份与前一个流行季完全相同,考虑到多数接种者的免疫力会随时间推移逐渐减弱,流感疫苗还是需要每年接种。 |
|
《关于公布可供对外出口的新型冠状病毒疫苗产品清单的公告》 |
2021-06 |
商务部 |
为确保疫苗产品质量与安全,提高贸易效率,我们支持列入清单的中国疫苗生产企业以自营方式组织出口,集中精力增加产品供应、稳定市场预期,让各国、特别是发展中国家都能用得上、用得起疫苗。 |
|
《关于进一步做好新冠病毒疫苗货物运输组织和服务保障工作的通知》 |
2021-04 |
交通运输部等 |
当前和未来一段时间,疫苗接种需求持续旺盛,特别是随着疫苗产能不断提升,疫苗及其原液、半成品跨区域运输保障任务日趋繁重。各地各部门要进一步提高政治站位,统一思想认识,强化责任担当,密切沟通协作,推动供需有效对接,优化运输组织调度和服务保障举措,加强运输全过程安全质量管控,完善应急处置措施,为疫苗生产、供应和接种提供坚实的运输服务保障。 |
|
《新冠病毒疫苗货物道路运输技术指南》 |
2021-01 |
交通运输部 |
切实保障新冠病毒疫苗货物安全便利运输。 |
|
《关于进一步严厉打击违法研制生产经营使用非洲猪瘟疫苗行为的通知》 |
2020-08 |
农业农村部 |
各省级畜牧兽医主管部门要组织对辖区内兽药经营企业开展全面检查,排查是否存在经营所谓“非洲猪瘟中试苗、自家苗、进口苗”等非法疫苗行为。 |
|
《疫苗生产车间生物安全通用要求的通知》 |
2020-06 |
科技教育司 |
利用病原微生物进行疫苗生产,具有一定的生物安全风险,需要在确保疫苗质量的同时,确保生产活动的生物安全。 |
|
《中华人民共和国疫苗管理法》 |
2019-07 |
药监局 |
加强监督检查,严厉打击疫苗药品领域违法行为。要牢固树立问题导向,坚持风险理念,统筹运用检查、检验、监测、投诉举报等手段排查风险,从源头防范疫苗质量风险。要做到对疫苗生产企业检查的高频次和全覆盖,依法严查重处违法违规生产行为。 |
资料来源:观研天下数据中心整理
此外,国家已经在不断加大免疫规划投入,例如:2022年十三届全国人大五次会议上国家卫生健康委指出,将重点推动条件成熟的地区率先出台免费HPV疫苗接种政策,不断提高适龄女孩HPV疫苗接种率。
资本端来看,新冠疫情后,行业开启资本化浪潮,相比几年前资本市场只有智飞、沃森两家疫苗企业,截至目前,具有重量级产品的万泰生物、康华生物已经完成IPO;康希诺生物股份公司成功登陆科创板,成为首个“A+H”疫苗股;此外,2021年6月25日,百克生物正式在上海证券交易所科创板上市。2021年9月,成大生物的科创板IPO获证监会批复。2022年1月12日,华兰生物子公司华兰疫苗创业板IPO申请获中国证监会批复。疫苗研发需要长期的人才资源及资金支持,我国疫苗产品相比海外发达国家产品力仍有提升空间,行业资本化一方面,可以助力相关企业创新发展。企业登陆资本市场之后,通过募集资金扩大规模,加大研发投入,推动技术创新,助力自身做大做强。另一方面,还可带动产业转型升级,提升我国疫苗相关产业国际竞争力,推动经济高质量发展。
产品端来看,目前国内疫苗的消费品种结构还有很大的发展空间,海外销售额较高的疫苗大品种如PCV13/20疫苗、HPV疫苗、带状疱疹疫苗等在我国量还相对较小,例如:带状疱疹疫苗目前全球仅上市3款,分别为GSK的欣安立适,默克集团的Zostavax以及SK化工株式会社的SkyZoster。其中,SkyZoster仅在韩国销售。Zostavax由于预防有效性低且市场竞争力疲弱,现已停产。目前中国本土有多家企业正在开发带状疱疹疫苗中,随着人口的老龄化以及带状疱疹新增病例数增加,其未来市场前景也仍被看好。
再比如HPV疫苗,由于目前适龄女性数量庞大,HPV疫苗供应紧缺,研究表明男性也可以从接种HPV疫苗中获益,预防生殖器疣、阴茎癌等,根据百度健康10月22日发布的《2020国民HPV防护图鉴》报告,与2015年相比,男性网民对“HPV疫苗”相关内容的搜索热度占比由原来的一成提升到如今的三成,未来如果从扩大适应症和整体消除HPV感染和宫颈癌的问题,男性的疫苗获批后,国内HPV疫苗男性适应症市场潜力有待开发和释放。另外如百白破-乙肝-灭活机会联合疫苗等品种还没有在国内上市,这些高价值大品种疫苗有很大的发展空间,例如:2023年预计康泰生物的人二倍体狂犬疫苗将获批上市、百克生物的带状疱疹疫苗获批上市、智飞生物的人二倍体狂犬、四价流感疫苗已获得I期临床试验总结报告有望在2022年底前获得受理等,相信随着国内企业的持续研发积累,国产大疫苗品种逐步上市,并将开启国产疫苗大品种时代。
2022年后部分国内疫苗企业预计上市产品
|
企业 |
疫苗产品 |
|
康泰生物 |
冻干人用狂犬病疫苗(人二倍体细胞) 冻干水痘减毒活疫苗 Sabin株脊髓灰质炎灭活疫苗(Vero 细胞) ACYW135脑膜炎结合疫苗 甲型肝炎灭活疫苗 重组肠道病毒71型疫苗(汉逊酵母) 吸附无细胞百日破(组分)联合疫苗 重组乙型肝炎疫苗(汉逊酵母) 吸附无细胞百日破灭活脊髓灰质炎和b型流感嗜血杆菌联合疫苗 吸附无细胞百日破灭活脊髓灰质炎联合疫苗 口服五价重配轮状病毒减毒活疫苗(Vero 细胞) 四价流感病毒裂解疫苗 60ug重组乙型肝炎疫苗(酿酒酵母) (免疫调节剂) |
|
智飞生物 |
三价流感病毒裂解疫苗 23价肺炎多糖疫苗 15价肺炎结合疫苗 冻干人用狂犬病疫苗(MRC-5细胞) 四价流感病毒裂解疫苗 ACYW135脑膜炎结合疫苗 冻干人用狂犬病疫苗(Vero 细胞) 福氏宋内氏痢疾双价结合疫苗 冻干重组结核疫苗(AEC/BC02) 肠道病素71型灭活疫苗 四价重组诺如病毒疫苗(毕赤酵母) 皮内注射用卡介苗 卡介菌纯蛋白衍生物 组份百白破疫苗 灭活轮状病毒疫苗 |
|
康希诺 |
13价肺炎球菌多糖结合疫苗(CRM197,TT 氧体》 吸附无细胞百(三组分)日破联合疫苗 |
|
沃森生物 |
重组肺炎球菌蛋白疫苗 TB-肺结核疫苗 ACYW135群脑膜炎球菌多糖结合疫苗 重组人乳头瘤病毒九价病毒样颗粒疫苗(6、11、16、18、3133、45、 52、58型L1蛋白) (毕赤酵母) (九价HPV 疫苗) 4价流感病毒裂解疫苗 重组EV71疫苗 伤寒Vi多糖疫苗 |
|
万泰生物 |
重组人乳头瘤病毒九价(6/11/16/18/31/33/45/52/58型)疫苗(大肠埃希菌) 水痘减毒活疫苗 水痘减毒活疫苗(VZV-7D) |
资料来源:各公司官网、医药魔方、观研天下数据中心整理
从发展空间来看,根据观研天下报告,2021年中国疫苗市场规模为991亿元,预计到2030年,国内疫苗市场规模有望达到3333亿元,同时,行业未来五年的年均复合增长率将在15%以上,是绝对的蓝海行业,但如何把握机遇,任重而道远。(LZC)

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。