一、儿童常用的药物种类丰富
儿童用药是维系儿童生命安全和保障儿童健康事业发展的重要支撑,对于满足儿科诊疗需求、防治各类儿童疾病、提高儿科医疗质量、提升儿童健康水平有着非常特殊的意义和价值。
儿童常用的药物类型

数据来源:观研天下整理
二、驱动因素分析
1、我国儿童人口基数庞大
按联合国“儿童权利公约”定义,儿童是指18岁以下的任何人,包括以下时期:新生儿/婴儿期(1岁以下)、幼儿期(1-3岁)、学龄前期(3-7岁)、学龄期(7-12岁)和青春期(12-18岁)。中国儿童的概念通常是指0-14岁的人群。目前,我国儿童人口基数庞大,根据国家统计局数据显示,2021年中国儿童人口数为2.5亿人,占全国总人口的比重17.95%。
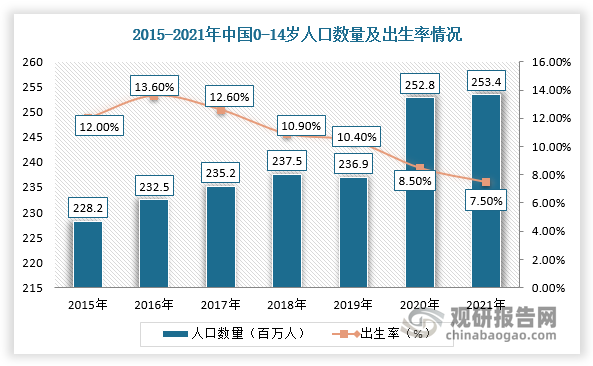
数据来源:观研天下整理
2、我国儿童患病率整体较高
同时,我国儿童患病率整体较高,儿童门诊人次占医院总门诊人次的近10%,且门诊量呈逐年上升趋势。现阶段,儿童患病的三大种类是呼吸系统疾病、消化系统疾病以及传染病。其中,儿童呼吸系统疾病患病率高居榜首,患病率高达近80%;其次是儿童消化系统疾病,最常见的疾病种类主要包括消化不良、儿童腹泻、肠胃炎等;传染病排名第三,主要疾病类型包括手足口病、肝炎等。
根据国家食品药品监督管理总局南方医药经济研究所发布的《2016年中国儿童用药安全调查报告》,在0-14岁儿童呼吸疾病患者群体中儿童有进行药物治疗的疾病患病率前五依次是感冒、发烧、咳嗽、消化不良、肠胃炎。

数据来源:观研天下整理
3、国家政策对儿童药研发的大力扶持
根据观研报告网发布的《中国儿科用药行业发展现状分析与投资前景预测报告(2023-2030年)》显示,近年来,国家不断出台相关政策来鼓励儿童药物的研发和生产,缓解国内儿童药物短缺问题,如2021年国家卫健委颁布了《国家基本药物目录管理办法(修订草案)》公开征求意见,本次修订的管理办法的基药范围中首次新增了“儿童药品”,由此可合理预计未来将有政策进一步保障儿童用药需求、促进儿童药的研发。
2020-2023年中国儿科药物行业相关政策汇总
|
名称 |
颁布时间 |
颁布部门 |
主要内容 |
|
《药审中心加快创新药上市许可申请审评工作规范(试行)》 |
2023.03.31 |
国家药监局药审中心 |
鼓励研究和创制新药,满足临床用药需求,结合抗疫应急审评过程中“早期介入、研审联动、滚动提交”等宝贵经验及监管科学行动计划形成的新工具、新方法、新标准,以制度形式转化、巩固和扩大抗疫成果,鼓励儿童用药、罕见病用药创新研发进程,加快创新药品种审评审批速度。 |
|
《生理药代动力学模型在儿科人群药物研发中应用的技术指导原则》 |
2023.03.28 |
国家药监局药审中心 |
鼓励在儿科人群药物研发过程中收集积累发育相关生理数据,以促进中国儿科人群药物的开发与研究。 |
|
《儿童抗肿瘤药物临床研发技术指导原则》 |
2023.03.24 |
国家药监局药审中心 |
对儿童抗肿瘤新药的临床研发提供思路和技术建议。 |
|
《关于进一步加强儿童临床用药管理工作的通知》 |
2023.01.16 |
卫健委 |
加强儿童用药遴选和配备管理,遴选儿童用药可不受“一品两规”和药品总品种数限制,进一步拓宽儿童用药范围,城市医疗集团、县域医共体等医联体要建立儿童用药联动管理机制,加强儿童用药目录的统一衔接,促进儿童用药在医联体内共享使用;强化儿童用药临床合理使用;加强药师配备并提供儿科药学服务;做好儿童用药处方调剂和专项点评;开展儿童用药临床监测;加强儿童用药指导和健康宣教。 |
|
关于印发《国家基本医疗保险、工伤保险和生育保险药品目录(2022年)》的通知 |
2023.01.13 |
国家医保局、人社部 |
及时做好支付范围调整;规范支付标准;扎实推动目录药品落地;规范民族药、医疗机构制剂、中药饮片的管理;对相关部门药品管理政策的支持,如国家基本药物目录、鼓励研发申报儿童药清单、鼓励仿制药目录内的药品等;目录外新增药品涉及23个临床组别,其中22个儿童用药。 |
|
《儿童用药口感设计与评价的技术指导原则(试行)》 |
2022.11.02 |
国家药监局药审中心 |
进一步鼓励儿童用药研发生产,满足儿童用药需求,保障儿童用药安全。 |
|
《关于进一步加强用药安全管理提升合理用药水平的通知》 |
2022.7.27 |
卫健委、国家中医药管理局 |
降低用药错误风险,提高用药安全水平,保障重点人群用药安全。医疗机构要针对老年人、儿童、孕产妇等特殊人群,强化用药安全管理。遴选儿童用药(仅限于药品说明书中有明确儿童适应证和儿童用法用量的药品)时,可不受“一品两规”和药品总品种数限制,增加用药范围,促进精准用药。 |
|
《中华人民共和国药品管理法实施条例(修订草案征求意见稿)》 |
2022.05.09 |
国家药监局 |
鼓励儿童用药品的研制和创新,支持药品上市许可持有人开发符合儿童生理特征的儿童用药品新品种、新剂型、新规格,对儿童用药品予以优先审评审批。在药物研制和注册申报期间,加强与申办者沟通交流,促进儿童用药品加快上市,满足儿童患者临床用药需求。对首个批准上市的儿童专用新品种、剂型和规格,以及增加儿童适应症或者用法用量的,给予最长不超过12个月的市场独占期,期间内不再批准相同品种上市。鼓励申请人在提交药品上市许可申请时提交儿童剂型、规格和用法用量等的研发计划。 |
|
《治疗儿科动脉性肺动脉高压药物临床试验技术指导原则》 |
2022.01.12 |
国家药监局药审中心 |
儿科动脉性肺动脉高压患者的病因、临床病程、以及治疗反应性等方面均与成人患者均存在一定差异,旨在指导儿科动脉性肺动脉高压的临床试验,提供可参考的技术规范。 |
|
《产业结构调整指导目录(2019年本)(2021修订)》 |
2021.12.30 |
发改委 |
鼓励推动儿童药、短缺药的研发、生产,着力提高短缺药品的供应保障能力;鼓励中药经典名方、中药创新药的开发与生产。 |
|
《注意缺陷多动障碍(ADHD)药物临床试验技术指导原则(试行)》 |
2021.09.13 |
国家药监局药审中心 |
缺陷多动障碍(ADHD)属于儿童常见精神障碍,旨在解决ADHD注意治疗药物缺乏,鼓励和推动ADHD药物研发,规范临床研究设计。 |
|
《儿童用化学药品改良型新药临床试验技术指导原则(试行)》 |
2021.09.13 |
国家药监局药审中心 |
鼓励对儿科用药进行改良,对化学药品改良型新药的分类、定义、临床试验指导等方面的逐级明晰。 |
|
《中国儿童发展纲要(2021-2030年)》 |
2021.09.08 |
国务院 |
加强儿童健康领域科研创新。围绕儿童重大疾病的预防、诊断、治疗、康复和健康管理开展基础研究和应用研究。加强儿科科技创新基地、平台建设,发挥儿科医学领域国家临床医学研究中心重要作用。鼓励儿童用药研发生产,加快儿童用药申报审批工作。完善儿童临床用药规范,药品说明书明确表述儿童用药信息。扩大国家基本药物目录中儿科用药品种和剂型范围,探索制定国家儿童基本药物目录,及时更新儿童禁用药品目录。推动儿童健康科技国际交流合作。 |
|
《化学药品和治疗用生物制品说明书中儿童用药相关信息撰写的技术指导原则(试行)》 |
2021.09.03 |
国家药监局药审中心 |
促进企业有序开展起草和完善药品说明书中儿童用药信息的相关工作,更好的指导临床合理用药。 |
|
《关于规范申请人儿童用药申报信息备注的通知》 |
2021.07.09 |
国家药监局药审中心 |
对涉及申报品种的儿童用药信息备注进行规范,在提交临床试验申请和上市申请时,由申请人在药品注册申请表中“其他事项”条目下备注:申请儿童专用药、申请新增儿童应用(适应症和用法用量)、本品属于鼓励研发申报儿童药品清单(写明批次和编号)。在提交补充申请时,由申请人在药品注册申请表中“补充申请的内容”条目下备注:申请新增儿童应用(适应症和用法用量)、申请修订儿童应用(适应症和用法用量)、申请增加儿童专用规格、申请修订说明书中儿童应用信息、申请其他与儿童应用相关的事项。 |
三、儿科药物行业市场规模呈现稳定增长趋势
目前,我国专业儿科药物种类匮乏且生产的医药公司数量少,2021年我国儿科药物市场规模占总医药市场规模的5.9%,低于同期的世界水平。并且,根据米内网数据,截至2022年5月我国获得批文的产品数约1.84万个,其中儿童药约930个,占比5%,品种较少;2021年我国儿童药只有1个规格的产品超过90%,规格少;3个规格以上的产品占比仅3%。
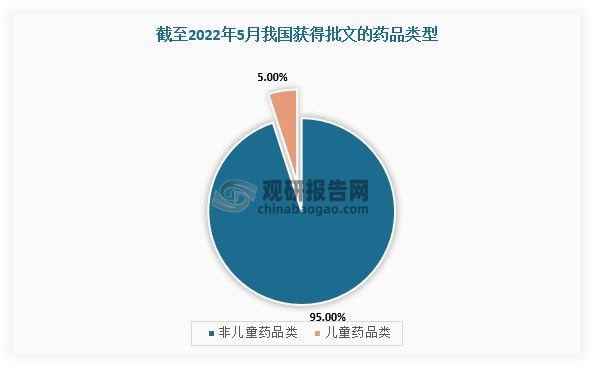
数据来源:观研天下整理
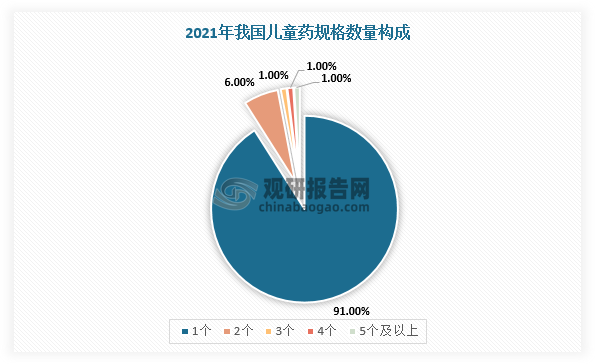
数据来源:观研天下整理
不过,随着人们对儿科疾病的重视程度提升和多项利好政策出台,我国儿科药物行业市场将快速增长。根据数据显示,2021年,我国儿科药物行业市场规模达1026亿元,2015-2021年复合增长率9.6%,预计2025年市场规模将达到1378亿元。
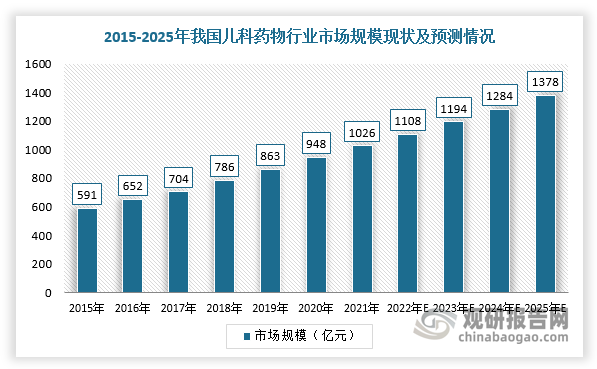
数据来源:观研天下整理(WYD)

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。