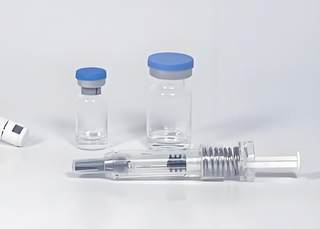
双特异性抗体是一种可以与相同或不同抗原上的不同表位结合的抗体结构,其可以桥接治疗剂(如T细胞、药物)及靶标(如肿瘤)或调节两种不同的病原体,以达到不同的治疗目的。双特异性抗体在自然界并不存在,需要通过重组DNA技术或细胞融合技术人工制备。与单克隆抗体相比,双抗增加了一个特异性抗原结合位点,因而特异性更强,可较准确靶向细胞并降低脱靶毒性,但双抗药物开发复杂性和技术壁垒更高,对于技术平台和靶点选择适配性要求也更高。
与单克隆抗体相比,双抗药物在组织渗透率、杀伤肿瘤细胞效率、脱靶率和临床适应症等指标方面具有较强的竞争力,临床应用优势显著。特别在使用剂量方面,由于其治疗效果可以达到普通抗体的100-1,000倍,使用剂量最低可降为原来的1/2,000,显著降低药物治疗成本,提高了市场空间。

资料来源:观研天下整理
近年随着生物技术的不断发展,针对双特异性抗体药物的研发热度提升显著,从而促使双特异性抗体技术不断创新和突破。截至2021年底,全球共有四款双特异性抗体获批上市,分别为卡妥索双抗(靶向CD3和EpCAM,2009年上市,2017年退市)、贝林妥欧单抗(靶向CD3和CD19,2014年上市)、艾美赛珠单抗(靶向FIX和FX,2017年上市)和Rybrevant(靶向EGFR和c-Met,2021年上市)。
同时单克隆抗体药物的快速发展和巨大成功,为双特异性抗体药物的发展奠定坚实的基础。在此背景下,全球双特异性抗体药物市场规模不断增长。但目前受到生物技术发展的限制,全球双特异性抗体药物市场发展还处于初步阶段。
数据显示,2020年全球双特异性抗体药物市场规模从2015年的1亿美元提升至27亿美元,复合增长率高达93.32%。预计未来全球双特异性抗体药物市场规模将保持高位增长,以46.79%的复合增长率于2025年增长至184亿美元。

数据来源:观研天下整理
我国双特异性抗体药物研发起步较晚,目前市场规模小。但2016年以来,双特异性抗体等创新药物研发进展迅速。目前国内共有300余款双抗在研药物,其中进入临床阶段的近百款。适应症方面,在已上市和在研药物中,肿瘤适应症占据多数,约占所有双抗药物数量的86.7%,排第二名的适应症为血液病,约占20.89%。
由于双特异性抗体技术壁垒较高,国内企业主要采用“合作引进+自主研发”的形式开发双特异性抗体,自2018年以来,中国双特异性抗体领域的投资和合作开发显著活跃,加快双特异性抗体药物的商业化进程。截至2021年底,国内共有两个进口双抗药品获批上市,分别为贝林妥欧单抗(靶向CD3和CD19,2020年上市)、艾美赛珠单抗(靶向FIX和FX,2021年上市)。与此同时,国内获批临床的双抗药品超过100个,其中康方生物PD-1/CTLA-4双抗已于2022年6月获批上市,双抗药物也将在2022-2023迎来第一波的上市潮,开始进入商业化竞争阶段。
尽管目前双特异性抗体药物在中国市场尚未取得明显的市场销售份额,但其发展潜力巨大。鉴于双克隆抗体是在单克隆抗体基础上发展催生的,单克隆抗体作为高端生物药品迅速崛起且市场表现良好,为双特异性抗体的商业化做出优秀示范,同时生物技术的发展推动生物药企积极布局双特异性抗体相关项目,特别是在政策法规的积极推动下,中国双特异性抗体药物的发展将进一步促进。预计到2025年,我国双克隆抗体药物市场规模将快速增长至121亿元,2021年至2025年的复合增长率达160.95%。

数据来源:观研天下整理
目前已有超30家企业布局双抗在研药物领域。其中处于Ⅲ期临床试验阶段的达到6款,包括恒瑞医药的SHR-1706(实体瘤适应症)、百济神州的ZW25(实体瘤适应症)、康宁杰瑞的KN026(2线HER2阳性胃癌适应症)和KN046(两个非小细胞肺癌适应症)、康方生物的AK112(两个非小细胞肺癌适应症),康方生物卡度尼利单抗的宫颈癌、胃癌适应症也进入到Ⅲ期临床试验。
根据观研报告网发布的《中国双克隆抗体药物行业发展趋势研究与未来投资分析报告(2023-2030年)》显示,我国双克隆抗体药物市场主要企业康方生物、恒瑞医药、康宁杰瑞、信达生物、再鼎医药、石药集团、复宏汉霖、泽璟制药、智翔金泰等企业。
我国双克隆抗体药物市场主要企业竞争优势情况
|
竞争优势 |
|
|
康方生物 |
产品集优势:公司目前拥有30个以上用于治疗肿瘤、自身免疫、炎症、代谢疾病等重大疾病的创新候选药物,其中17个新药进入临床研究,13项关键/III期临床试验正在开展,3个新药实现商业化销售(含1个对外授权)。 |
|
商业体系优势:公司打造了独有的以端对端康方全方位探索平台(ACE Platform)和双特异性抗体开发技术(Tetrabody)为核心的一体化研发创新体系、国际化标准的GMP生产体系和运作模式先进的商业化体系。 |
|
|
产品优势:2021年8月,安尼可®(PD-1单抗,派安普利单抗注射液)获批上市。2022年6月,公司全球首创的肿瘤双免疫检查点双抗开坦尼®(PD-1/CTLA-4双抗,卡度尼利单抗注射液)获批上市。2022年12月,公司另一个自主研发的全球首创双抗依沃西(PD-1/VEGF双抗,AK112),以5亿美金首付款、总交易额高达50亿美金和销售净额低双位数比例提成的合作方案,授予Summit Therapeutics于美国、加拿大、欧洲和日本的开发和商业化独家许可权。 |
|
|
康宁杰瑞 |
平台优势:公司创建了具有自主知识产权的生物大分子药物发现、研发、生产技术平台,包括蛋白质/抗体工程平台、抗体筛选平台和多功能抗体开发平台。 |
|
产品管线优势:康宁杰瑞开发出了丰富的产品管线,具有显著的差异化特点和强大的全球竞争力:其中1个产品KN035(恩沃利单抗注射液,全球首个皮下注射的PD-L1抑制剂;商品名:恩维达®)获批上市;2个产品入选国家“重大新药创制”专项;3个产品获美国FDA授予4项孤儿药资格;3个产品进入多项Ⅲ期或关键性临床研究。 |
|
|
生产优势:公司在苏州工业园区建设了生物大分子药物研发与产业化基地。生产基地占地75亩,按照NMPA、FDA和EMA的GMP标准建设,总设计规模超4万升。Ⅰ期产能已上线,获得生产许可证,通过欧盟QP和美国客户的审计,可为肿瘤患者提供安全、疗效好、成本可控的创新药。 |
|
|
恒瑞医药 |
品台优势:公司具有行业领先的制药全面集成平台,已前瞻性地广泛布局多个治疗领域,并向纵深发展。同时产生了一批具有自主知识产权、国际一流的新技术平台,如蛋白水解靶向嵌合物(PROTAC)、分子胶、抗体偶联药物(ADC)、双/多特异性抗体、基因治疗、mRNA、生物信息学、转化医学等。 |
|
多元化发展优势:公司在肿瘤领域有丰富的研发管线,覆盖激酶抑制剂、抗体偶联药物(ADC)、肿瘤免疫、激素受体调控、DNA修复及表观遗传、支持治疗等广泛研究领域,针对多靶点,深耕组合序贯疗法,力求高应答、长疗效。与此同时,公司在自身免疫疾病、疼痛管理、心血管疾病、代谢性疾病、感染疾病、呼吸系统疾病、血液疾病、神经系统疾病等领域也进行了广泛布局。 |
|
|
研发优势:公司建立了国家级企业技术中心和博士后科研工作站、国家分子靶向药物工程研究中心、“国家重大新药创制”专项孵化基地。 |
|
|
质量优势:公司建有高标准的生产基地,形成了分工明确、统一协作的生产体系,依据中国GMP、美国cGMP、欧盟GMP、ICH等国内外质量管理法规要求建立了完善的质量管理体系文件和管理制度并持续改进。在质量标准严格遵从国家法定标准的基础上,还对部分关键质量指标进行严控和提高,制定了高于法定标准的企业内控标准。 |
|
|
市场优势:公司始终坚持“科学为本,患者至上”的宗旨,在抗肿瘤药、手术麻醉类用药、造影剂、特殊输液、心血管用药等领域建立了专业化的学术队伍,依托专业化医学研究和学术推广,搭建多样化的学术交流平台,传递最新的医药研究成果,支持药物的安全风险管理,为广大患者与医疗工作者提供有效快捷的治疗方案、专业的学术支持与服务,已成为我国抗肿瘤、麻醉等领域的市场领跑者。 |
|
|
信达生物 |
产品链优势:公司建立起了一条包括35个新药品种的产品链,覆盖肿瘤、自身免疫、代谢、眼科等多个疾病领域,其中7个品种入选国家“重大新药创制”专项。 |
|
研发优势:信达生物已组建了一支具有国际先进水平的高端生物药开发、产业化人才团队,包括众多海归专家,并与礼来、罗氏、赛诺菲、Adimab、Incyte和MD Anderson 癌症中心等国际合作方达成28项战略合作。 |
|
|
药物进程优势:公司已有 8个产品获得批准上市,它们分别是信迪利单抗注射液(达伯舒®),贝伐珠单抗注射液(达攸同®),阿达木单抗注射液(苏立信®),利妥昔单抗注射液(达伯华®),佩米替尼片(达伯坦®),奥雷巴替尼片(耐立克®), 雷莫西尤单抗注射液(希冉择®),塞普替尼胶囊(睿妥®),3个品种在NMPA审评中,6个新药分子进入III期或关键性临床研究,另外还有18个新药品种已进入临床研究。 |
|
|
再鼎医药 |
产品管线优势:。再鼎医药凭借经验丰富的团队,已打造起由创新的临床后期候选药物组成的广泛产品管线,其中有四款疗法已在中国上市。 |
|
品牌优势:再鼎医药成为了寻求进入中国市场以及寻找国际临床开发长期战略合作伙伴的全球生物制药公司“值得信赖的合作伙伴”。 |
|
|
生产优势:公司还拥有小分子和大分子生产基地、经验丰富的注册事务团队以及高度专业的商业化团队,负责创新产品的生产、注册和商业化。 |
|
|
全球化布局优势:公司目前在上海设有总部和研发中心,在北京设有临床和注册事务办公室,在苏州设有全球生产和研发基地,在中国香港、台湾和广州设有商业化办公室,在美国旧金山和剑桥设有办公室。 |
|
|
人才优势:截至2023年3月31日,公司在全球拥有大约2100名员工。 |
|
|
研究优势:再鼎医药是一家拥有从早期药物发现、临床研发、生产到商业化能力的全面整合的生物制药公司。公司的内部研发中心,致力于创新药物的研发,加强药物研发管线;强大的临床开发团队,目前管理超过50项正在进行或计划进行的临床研究。 |
|
|
石药集团 |
生产优势:目前公司在冀、晋、鲁、苏、赣、津等省市设有10余个药品生产基地。 |
|
市场优势:公司产品销售遍及全球100多个国家和地区。 |
|
|
销售优势:公司有36个品种单品种销售过亿元。 |
|
|
复宏汉霖 |
产品优势:公司产品覆盖肿瘤、自身免疫疾病、眼科疾病等领域,已在中国上市5款产品,在国际上市1款产品,18项适应症获批,3个上市申请分别获中国药监局、美国FDA和欧盟EMA受理。 |
|
产业链优势:自2010年成立以来,复宏汉霖已建成一体化生物制药平台,高效及创新的自主核心能力贯穿研发、生产及商业运营全产业链。 |
|
|
生产优势:。公司已建立完善高效的全球创新中心,按照国际药品生产质量管理规范(GMP)标准进行生产和质量管控,不断夯实一体化综合生产平台,其中,上海徐汇基地已获得中国和欧盟GMP认证,松江基地(一)也已获得中国GMP认证。 |
|
|
产品管线优势:复宏汉霖前瞻性布局了一个多元化、高质量的产品管线,涵盖20多种创新单克隆抗体,并全面推进基于自有抗PD-1单抗H药汉斯状®的肿瘤免疫联合疗法。 |
|
|
产品优势:继国内首个生物类似药汉利康®(利妥昔单抗)、中国首个自主研发的中欧双批单抗药物汉曲优®(曲妥珠单抗,欧洲商品名:Zercepac®,澳大利亚商品名:Tuzucip®和Trastucip®)、汉达远®(阿达木单抗)和汉贝泰®(贝伐珠单抗)相继获批上市,创新产品汉斯状®(斯鲁利单抗)已获批用于治疗微卫星高度不稳定(MSI-H)实体瘤、鳞状非小细胞肺癌和广泛期小细胞肺癌,成为全球首个获批一线治疗小细胞肺癌的抗PD-1单抗,其食管鳞状细胞癌适应症的上市注册申请也正在审评中。 |
|
|
智翔金泰 |
技术优势:公司基于新型噬菌体呈现系统的单抗药物发现技术平台和双特异性抗体药物发现技术平台不断迭代,技术先进且非常成熟。 |
|
研发优势:公司通过持续跟踪药物临床开发阶段的各项反馈,有针对性的加强自身研发实力,并根据全球药物靶点前沿发展动向,结合自身技术特点,动态调整药物研发方向,不断迭代演进,驱动企业保持持续创新。 |
|
|
产品研发进度优势:公司未来几年预计上市的产品为 GR1501、GR1801 和 GR1802,其中 GR1501为国内企业首家提交新药上市申请的抗 IL-17 单克隆抗体注射液,GR1801 为国内企业首家狂犬病被动免疫双特异性抗体药物,GR1802 为国内企业第二梯队进入中重度哮喘 II 期临床试验的抗 IL-4Rα 单克隆抗体注射液,上述产品均存在巨大的临床需求,市场空间广阔。除上述产品外,公司在研产品 GR1603 是国内企业首家进入临床试验阶段的抗 IFNAR1 单克隆抗体药物,GR1901 是国内企业首家获批临床的 CD123×CD3双特异性抗体药物,GR1803 的研发进度在国内企业也排名靠前。 |
|
|
泽璟制药 |
产品优势:公司积极开发具有全球领先性和竞争力的系列抗肿瘤抗体新药产品,包括多个双/三特异性抗体ZG005、ZG006、ZGGS18、GS15、GS11和ZGGS001等。其中ZG005已获得中国和美国的临床批准,ZGGS18的IND申请已获FDA和中国药监局批准;预计多个抗体产品将于2022-2023年申报中国和美国的IND。 |
|
产品管线优势:公司注重同时布局大病种疾病和罕见病,注重在研药品的领先性、可及性、广谱性或特效性,从而形成产品管线的差异化综合竞争优势。 |
|
|
产品研发进程优势:与同类多数新药研发公司相比,公司的重要特点是多个不同治疗领域的产品管线已进入或即将进入商业化阶段。 |
|
|
技术优势:建立了小分子药物研发和产业化平台和复杂重组蛋白生物新药和抗体新药研发及产业化平台,公司及子公司GENSUN进一步建立了研发肿瘤免疫治疗抗体药物的技术能力。 |
|
|
研发优势:公司拥有包括药物靶点筛选与机理验证、化合物分子设计与筛选、临床前研究、CMC、临床方案设计与执行、药品生产和质量控制、新药注册申报等在内的完整的研发体系,科技创新能力突出。 |
资料来源:观研天下整理(WW)

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。